
Energía libre de Gibbs
En termodinámica, la energía libre de Gibbs (o entalpía libre) es un potencial termodinámico, es decir, una función de estado extensiva con unidades de energía, que da la condición de equilibrio y de espontaneidad para una reacción química (a presión y temperatura constantes).
La segunda ley de la termodinámica postula que una reacción química espontánea hace que la entropía del universo aumente, 0 " src="http://upload.wikimedia.org/math/9/b/d/9bdeab2f0a75563fe467ade61ff65353.png">, así mismo
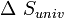 esta en función de
esta en función de  y
y  .Por lo general solo importa lo que ocurre en el sistema en estudio y; por otro lado el cálculo de
.Por lo general solo importa lo que ocurre en el sistema en estudio y; por otro lado el cálculo de  puede ser complicado. Por esta razón fue necesario otra función termodinámica, la energía libre de Gibbs, que sirva para calcular si una reacción ocurre de forma espontánea tomando en cuenta solo las variables del sistema.
puede ser complicado. Por esta razón fue necesario otra función termodinámica, la energía libre de Gibbs, que sirva para calcular si una reacción ocurre de forma espontánea tomando en cuenta solo las variables del sistema.
No hay comentarios:
Publicar un comentario